疫苗获批,中国全民免费接种:大流行终结开始?
原标题:新冠待解|疫苗获批,中国全民免费接种:大流行终结开始?
2020年的最后一天,中国作为全球人口第一大国,郑重承诺将为全民免费提供新冠疫苗。自2019年年底,新冠大流行阴影一直笼罩在人类头顶,中国政府的这一承诺犹如一道曙光,拨云见日。
当天举行的国务院联防联控机制新闻发布会上还传来重磅消息:国药集团中国生物新冠灭活疫苗已获得国家药监局批准附条件上市。这意味着始终处于全球新冠疫苗研发第一方阵的中国疫苗将“有资格”助力全球重启。
截至目前,COVID-19大流行席卷全球已一年有余,近180万患者付出了生命,全球经济和社会遭受重创,人类在保持社交距离和常戴口罩中期待疫苗已久。但疫苗研发从来不是一件因外界期待就能一蹴而就的工作。
发布会上,国家卫健委副主任、国务院联防联控机制科研攻关组疫苗研发专班负责人曾益新描述了中国第一支附条件上市新冠疫苗的诞生之路:4月2日,全球第一个新冠灭活疫苗获批开展Ⅰ、Ⅱ期临床试验,到6月23日,全球第一个启动Ⅲ期临床试验,再到6月24日,经过严格的程序,依法依规审批开展紧急使用。再到7月份以来,多个疫苗陆续到境外去开展Ⅲ期临床试验。再到今天第一个疫苗附条件上市,我国的疫苗研发工作始终处于全球第一方阵。
“在疫苗研发生产过程中,我们始终把疫苗的安全性、有效性放在第一位。”曾益新强调。值得期待的是,中国的新冠疫苗还有着更多“后备军”,到目前为止,中国5条技术路线14个疫苗已经进入临床试验,其中3条技术路线5个疫苗进入III期临床试验。
康希诺生物股份公司董事长兼总经理宇学峰在接受澎湃新闻记者采访时曾表示,过去的这一年里有太多的没想到,“有的时候,突发公共卫生事件确实是防不胜防,所以我们要建立一些技术平台,我们希望能够最快的速度开发出疫苗来。”
宇学峰同时说,“但是说句心里话,从开发埃博拉疫苗那会儿开始,我之前就没想到我们会去做埃博拉。你会考虑到像SARS、MERS都是冠状病毒,但你知道新冠病毒会是什么特点吗?你也不可能去提前判定有这么一个东西。”
康希诺和军事医学研究院陈薇院士团队联合研发的腺病毒载体新冠疫苗在全球率先开展临床研究,是全球首个进入临床研究阶段的新冠疫苗。
双方此前还合作开发埃博拉疫苗。“我们必须时刻有这种打‘遭遇战’的准备,平常要把自己的技术平台、科学思路要理顺,要有足够的资源和能力,你才能够尽快地把这个事情做起来,”宇学峰说。
回望这一年,全球新冠疫苗的研发实际上堪称“闪电速度”。顶级学术期刊《自然》(Nature)近日刊发的一篇报道分析,这可能深刻改变疫苗科学的未来。这得益于一些新技术的成熟,更得益于从未有过的人力和资金的集中投入。
疫苗的使用是否会成为全球疫情防控的根本转折点?毕竟,在过去的100多年中,人类公共卫生领域取得的两个最重要的成就:一个是卫生,另一个就是疫苗。
在前后两任中科院武汉病毒研究所所长胡志红、陈新文主编的《普通病毒学》一书中,他们是如此解释这两大路径的重要性的:卫生的改进大大减少了人类与病原微生物的接触和感染;疫苗接种则主动加强了人体预防病原微生物的入侵感染和由其引发的疾病。
这两大进步显著降低了人类因传染病而导致的死亡率。
不过,目前这些根据紧急使用条例批准、附条件批准的首批新冠疫苗也将受到持续监测,具有公共安全属性的它们不容出现纰漏。
另外,在目前的全球疫情大流行下,疫苗的投入使用并不意味着可以立即放松警惕。疫苗本身会遭遇它的强敌:病毒突变。近期在欧洲多国出现的新冠变异毒株B.1.1.7已开始引发外界对此的担忧。
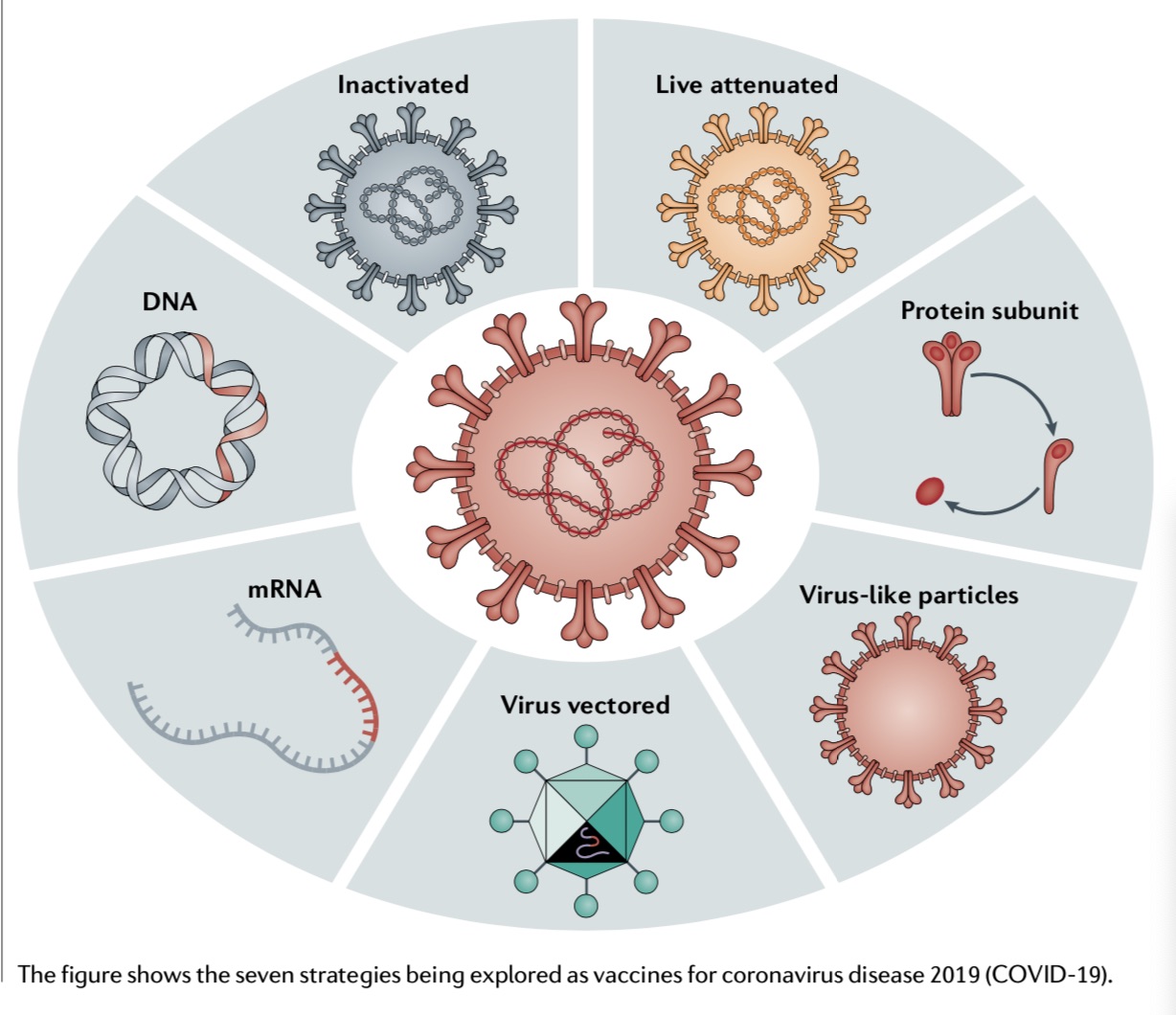
7种研发中的新冠疫苗类型。图片来源:中科院院士、中国疾控中心主任高福等人论文“Viral targets for vaccines againstCOVID-19”。
史无前例的“闪电开发速度”
疫苗是希望。中科院院士、中国疾控中心主任高福等人近日在《自然综述-免疫学》发表了一篇题为“Viral targets for vaccines againstCOVID-19”的进展综述论文,开篇写道:COVID-19已经蔓延到220个国家或地区,导致广泛的社会和经济破坏。迫切需要研制一种安全有效的疫苗,以帮助结束这一大流行。
但要知道的是,病毒作为地球上丰度最高的生物,其数量超过所有细胞生物至少一个数量级,能消灭或者遏制病毒的疫苗至今仍然有限。
但作为预防感染性疾病最经济也是最有效的方法,科学家在研制疫苗方面孜孜不倦。近代疫苗学先河由英国著名科学家爱德华·詹纳(Edward Jenner)开创,1798年,乡村行医多年的他非正式发表了《天花疫苗的因果之调查》一书,23个种痘而不再患天花的病例被记录了下来,牛痘预防天花的方法随后在全球广为接受。
发现这一方法有效只是开始,詹纳的贡献更在于通过试验证明接种牛痘后再人为让受试者感染天花病毒但不会致病。他将此过程称为“接种疫苗”(vaccination),第一次确立了“疫苗免疫”的概念。詹纳因此被公认为免疫学之父。
当然,比詹纳早1000多年,中国人就在世界上首创“种痘(人痘法)”来预防天花,这被称为“类疫苗”医学实践。遗憾的是,中国的这一实践,没有获得理论上的认识突破。不过有趣的是,詹纳在其8岁时也接种过人痘。
詹纳创立近代疫苗学180多年后的1979年10月,世界卫生组织(WHO)在肯尼亚首都内罗毕宣布“全世界已经消灭了天花”,这也是人类疫苗史上最辉煌的篇章。
疫苗学发展了2个多世纪后,开发疫苗有了一套成熟的步骤。宇学峰在接受澎湃新闻记者采访时表示,“疫苗研发是一个很繁杂的系统性的工程,不是说一蹴而就的。”
疫苗研发过程一般分为实验室发现、临床前研究和临床试验三个阶段,随后还有上市批准环节。
在此次新冠之前,疫苗的这一周期平均需要8-20年。而此前的最快疫苗纪录是在上世纪60年代创下的,当时科学家从获取腮腺炎病毒毒株到最终疫苗获批用了4年。
但此次的新冠疫苗创下了新的历史,被称为是疫苗开发史上的“闪电开发速度”。和H5N1、H7N9、埃博拉病毒、寨卡病毒等作战多年的中科院微生物所研究员施一对澎湃新闻记者表示,“今年疫苗的推动其实是非常快的,比我们正常的疫苗推进得快了很多。”
“不计成本”投入的“并联”模式
全球疫苗闪电速度研发背后离不开中国科研人员的努力。中国科学院院士、中国疾控中心主任高福2020年12月29日接受新华社采访时表示,“首先我们中国将分离出来的病毒、测序结果都向世界公开透明了,很快进入了新冠肺炎疫苗的研发。”
从全球范围来看,自2020年12月以来,辉瑞/BioNTech、莫德纳、牛津/阿斯利康疫苗的新冠疫苗先后在国外获紧急使用授权;在国内,国药集团中国生物新冠灭活疫苗也已获得国家药监局批准附条件上市。
佛罗里达大学的生物统计学家Natalie Dean在接受《自然》采访时说,这种研发速度“挑战了我们开发疫苗的可能性的整个范式”。科学家希望可以用相似的时间来生产其他疫苗,而这有着重大的现实意义。
哈佛医学院病毒学和疫苗研究中心主任Dan Barouch也表示,新冠疫苗的开发经验肯定会改变疫苗科学的未来。他说,“这表明,在真正威胁全球的紧急情况下,如果有足够的资源,疫苗开发可以快速进行。”
我们再去分析快速研发背后的一些主要原因,不难发现大量的科研力量和资金的投入是一个大前提。而此外重要的一点是,和其他疫苗的常规推进相比,新冠疫苗的研发过程还进行了并联。
复旦大学病原微生物研究所所长姜世勃此前详细解释了什么叫“并联”。
他表示,我们按正常程序一个疫苗研究从最初抗原制备到动物免疫、中和活性鉴定、动物攻毒保护实验、动物安全性评价到临床试验,一直到规模化生产,这整个过程可能需要四至五年甚至十几年才能完成。“但是现在我们希望能在一年之内完成这些工作,所以不能按照常规的方法进行。”
姜世勃表示,常规方法是循序渐进,一步完成以后再进行第二步、第三步,现在是多个团队在同时进行,有人在检测中和活性,另外有人做动物攻毒实验、动物安全性评价以及临床研究,多个团队同时进行就是将串联改成并联。
这种方式显然是“不计成本”的。姜世勃表示,这是有一个风险非常大的研发策略,比如一个团队在动物攻毒实验的时候发现这个疫苗没有保护效果,而其他团队已经完成的工作,如规模化生产等这些部分都前功尽弃了,可能会损失很多经费。“所以,只有在特殊情况下才能采取这种策略。”
葛兰素史克公司的疫苗部门首席科学家Rino Rappuoli表示,一些公共投资和私人慈善家会给疫苗公司投入一大笔资金,他们可以做临床前和I期、II期和III期临床试验以及生产,并行推进而不是按顺序推进。这意味着,企业可以押注于开始大规模测试和生产可能行不通的候选疫苗。伦敦卫生与热带医学学院疫苗中心主任坎普曼说,“这完全降低了整个开发过程的风险。”
为什么要关注ADE?
疫苗面向的是健康人群,“安全有效、质量可控”是疫苗开发必须遵循的原则。“闪电开发速度”速度下的新冠疫苗,全球科研力量、资本和监管方都为其冲刺开绿灯,这是否会在这些原则上打折扣?
此前,阿斯利康、强生的新冠疫苗均因试验者出现无法解释的疾病暂停临床研究,一度引发外界对新冠疫苗的担忧。一名接受澎湃新闻记者采访的传染病专家提醒,我们需要关注3个风险因素,“第一,严重的自身免疫反应,如横断性脊髓炎、格林巴利综合征、急性播散性脑脊髓炎等,均可由疫苗引起;第二,抗体依赖增强(ADE),可能使疾病更加严重;第三,迅速丧失免疫保护能力。”
“我们必须承认,我们对这种新型冠状病毒疫苗知之甚少。”该传染病专家提醒。
施一在接受澎湃新闻记者采访时也提到,“我们所担心的就是它的一个安全性,会不会引来一些副作用?”这也是大多数人关注的问题。
他提到的一点即为广泛讨论的抗体依赖增强作用(ADE)。ADE表现为在疫苗免疫一段时间后,病毒再次感染人体时病毒的复制不会被抑制反而会被促进,意味着一部分人在接种了疫苗之后,其自身产生的一些非保护性抗体会导致疾病的加重。
另一名病毒学家在接受澎湃新闻记者采访时也提到ADE现象,他以登革热(DF)中存在的这一现象提醒,“新冠疫苗的研发要充分考虑这一副作用。”登革热是一种蚊媒传染病,主要在热带和亚热带地区流行,严重时可致死亡。登革病毒为单股正链RNA病毒,对登革病毒来说,让人恐怖的是二次感染,在部分人群中,第一次感染后产生的非中和性抗体可促进非同一血清型病毒感染,进而加重病情,也就是所谓的ADE,导致很可能致命的登革出血热和登革休克综合征。
而在SARS时期,科学家也曾在猴子身上做过SARS病毒疫苗测试,结果是存在ADE现象,但后来因为疫情的终止而中断了相关疫苗的研发。加州大学伯克利分校
科学界也希望这种担忧是“杞人忧天”。
美国加州大学伯克利分校公共卫生学院博士后学者Leah Katzelnick等人在《传染病杂志》(The Journal of Infectious Diseases)发表过一篇题为“COVID-19 Vaccines: Should We Fear ADE?”的综述文章。他们对新冠疫苗是否会导致ADE的结论是“不可能”。
Katzelnick等人解释称,因为人类冠状病毒疾病缺乏如登革病毒那样的ADE的临床、流行病学、生物学或病理属性特征。他们称,“与登革病毒不同,SARS和MERS冠状病毒主要感染呼吸道上皮,而不是巨噬细胞。重症疾病主要针对有基础疾病的老年人,而不是婴儿或有冠状病毒感染史的人群。”但他们同时指出,接种SARS或MERS疫苗的动物再次感染活病毒会导致疫苗过敏反应(VAH),“安全有效的COVID-19疫苗必须避免VAH。”
值得一提的是,从另一个角度来说,ADE等副作用该不该成为新冠疫苗开发的“刹车”?科学界和相关疫苗企业也有不同的观点。
施一谈到,针对新冠病毒的疫苗研发也有这方面(ADE)的思考,而截至目前科学界也无法完全排除新冠疫苗会产生ADE的可能性。“我们还没法判断,因为ADE的发生是你打完疫苗过了一年左右的时间,当你的保护性抗体水平下降的时候才可能会产生的一个效应,那么现在我们的疫苗都还没有到这个时间,所以我们现在还没法去评估它是不是会产生ADE副作用。”
施一强调,“我们没法等待太多,因为现在很多国家已经隔离了很长一段时间了,国与国之间的交流基本也是断的。”从这一角度考虑,他认为还是要推动一些疫苗具体往下走,如果未来保护性抗体水平发生下降,我们可以通过再次接种疫苗来加强免疫保护。
宇学峰则对澎湃新闻记者表示,目前来说大家还没有真正在人身上观察到ADE这个问题,“我们也在和国际上的一些专家,包括WHO的专家们也在交流,我们会随时关注这个问题,但是我们不认为现在大家因为担心可能出现这个问题而缩手缩脚。”
前述传染病专家在接受澎湃新闻记者采访时表示,“这是历史上首次对人类冠状病毒疫苗进行测试,我们无法预料会引发多少自体免疫反应,我们必须对所有的可能性持开放的态度。”

在研新冠疫苗主要靶点。图片来源:中科院院士、中国疾控中心主任高福等人论文“Viral targets for vaccines againstCOVID-19”。
过敏反应等比较严重的不良反应发生率大约为百万分之二
曾益新在国新办新闻发布会上提到,“在疫苗研发生产过程中,我们始终把疫苗的安全性、有效性放在第一位。”
他介绍道,为了保护高风险人群,2020年6月份,按照依法依规批准的《新冠病毒疫苗紧急使用方案》,我们采取小范围起步、稳妥审慎、知情同意自愿的原则,在充分的不良反应监测和应急救治准备的前提下,对高风险人群开展了新冠疫苗的紧急接种。到2020年11月底,累计接种超过了150万剂次,其中约6万人前往境外高风险地区工作。
随后,为了防范冬春季节的疫情暴发,也为了有效保护冷链物流人员、海关边检人员、医疗疾控人员、公共交通人员,以及农贸市场、海鲜市场等一些感染风险相对比较高的人群,中国于12月15日正式启动了我国重点人群的接种工作。半个月来,全国重点人群累计接种已经超过了300万剂次。
曾益新表示,这次的300万,加上之前的150万,“充分证明了我们的疫苗安全性良好。”他同时介绍道,当然也发生了一定比例的不良反应,总的发生率,跟常规接种的那几种灭活疫苗很接近,主要的表现是一些局部的疼痛、局部的硬结这样一些情况。轻度发热的病例大概不到0.1%,过敏反应等比较严重的不良反应发生率大约为百万分之二。“这些情况经过及时处理,都得到了很好的治疗。”
施一也对澎湃新闻记者表示,未来新冠疫苗仍需要长期追踪。“疫苗的保护性能够持续多长时间,这个是我们需要持续跟踪的。当疫苗接种完以后,在一年或者是更长时间里头,它有没有可能会产生副作用,这也是我们需要思考的。”
不只考虑安全性和有效性
除了长期监测疫苗上市后的不良反应,我们还面临着其他问题。
国务院联防联控机制科研攻关组疫苗研发工作组组长郑忠伟在前述发布会提到,“评价一个疫苗有很多的指标,但是我想,非常重要的指标包括安全性、有效性、可及性、可负担性,其中安全性和有效性是最重要的两个评价指标。”
除了疫苗的安全性、有效性以外,“疫苗的可及性、可负担性也是需要我们关注的。”郑忠伟表示,因为只有一个疫苗在安全性、有效性有保障的前提下,它的可及性、可负担性均比较好的情况下,这支疫苗才能真正成为公共产品。
值得注意的是,不同形式的疫苗因其自身特点各有优缺点。前述传染病专家对澎湃新闻记者表示,“我们不需要进行任何特定形式的疫苗接种,也不要过早下结论。”
高福等人在上述提到的综述文章中,全球新冠疫苗的开发主要基于7条技术路线,即灭活疫苗、减毒疫苗、病毒载体疫苗、蛋白亚单位疫苗、DNA疫苗、RNA疫苗、纳米颗粒疫苗。郑忠伟在前述发布会上也提到,具体到说哪个疫苗更好,或者说我国疫苗和国外的疫苗哪个更好,我觉得不能简单地进行评价。因为各条路线的疫苗各有优势,这也是我们当初在疫苗研发过程中布局五条技术路线的原因。
郑忠伟强调,我们只有综合判定每一个疫苗的安全性、有效性、可及性、可担负性,才能对这个疫苗作出科学评价。“像现在正在推进研发的灭活疫苗、重组蛋白疫苗,已经经过了数十年甚至上百年,数十亿甚至上百亿人次的使用,它的安全性、有效性、可及性得到了时间的检验,也得到了科学验证。但是随着人类科技的进步,随着人类社会的发展,随着一系列新技术、新方法应用于疫苗研发,未来一定会有应用新技术、新方法研制出来的疫苗,在安全性、有效性、可及性等方面做得更好。”
施一对澎湃新闻记者表示,没法去直接评判哪种疫苗最为合适。“只能说哪一款疫苗最合适我们国家,我们就往下推。这里面不仅考虑它的有效性和安全性,甚至还要考虑它的可及性、生产能力等。”
而一些顶级期刊也在开始关注疫苗的可及性问题。《柳叶刀传染病学》(The Lancet Infectious Diseases)在线发表的一篇专门讨论了新冠疫苗的公平分配问题。这一文章乐观开篇:如果一切按照计划进行下去,2020年底会是COVID-19终结的开始。
但英国帝国理工学院的研究助理Zolta n Kis对辉瑞新冠疫苗评价道,“物流需求对它而言是非常具有挑战性的。”就这支疫苗本身,它并没有能力终结大流行,因为它不可能在全世界建立一个超冷链。辉瑞新冠疫苗需要零下70摄氏度的储存环境,据称这种疫苗若在超低温环境下储存,最多可保存6个月;而放入普通冰箱后,疫苗的保质期仅为5天。相比之下,环境温度变化对灭活疫苗的免疫原性影响较小,因此灭活疫苗对冷链运输要求较低。
Kis认为,在发达国家中,辉瑞新冠疫苗比较适合大城市,因为大城市有储存能力,可以在几天内运送大批人接种疫苗。
成本与公平
而成本也可能是一个问题。此前的公开报道就可以看到,一些高收入国家已经与制药公司签署优先采购协议,以确保未来疫苗供应。而对非洲等贫穷国家来说,最佳的机会可能是参与“新冠肺炎疫苗实施计划”(COVAX)。
COVAX是全球疫苗免疫联盟(GAVI)、流行病防范创新联盟(CEPI)和世卫组织之间的一项联合倡议,其任务是确保新冠疫苗得到公平和公平的分配,目标是到2021年底生产20亿剂疫苗,并将其中一半用于包括非洲一些国家在内的低收入国家。世卫组织非洲区域主任Matshidiso Moeti表示,“COVAX是一项开创性的全球倡议,它将确保非洲国家不会被排在获得新冠疫苗队伍的最后。”
辉瑞的BNT162b2新冠疫苗目前还不在COVAX疫苗计划的供应商名单中,其初始价格为每剂近20美元。据路透社此前报道,WHO正在与辉瑞谈判,希望将其新冠肺炎疫苗纳入早期全球推广计划。
阿斯利康则已加入COVAX,其开发的新冠疫苗可储存在2-8摄氏度,价格为每剂3-4美元,并承诺将永久性地为发展中国家保持低价格。阿斯利康公司估计,到2021年其生产能力将达到30亿剂。
中国已于2020年10月宣布加入COVAX,并表示疫苗研发完成并投入使用后,愿作为全球公共产品,率先惠及发展中国家尤其是非洲国家。在前述新闻发布会上,外交部国际司负责人申博也表示,中国新冠疫苗研发完成并投入使用后,将坚定履行承诺,将疫苗作为全球公共产品,以公平、合理价格向世界供应。
“我们也始终高度重视疫苗在发展中国家的可及性和可负担性,将根据具体情况,积极考虑以多种方式向发展中国家提供疫苗,包括捐赠和无偿援助等。我们也呼吁国际社会一道,共同推动全球疫苗的公平分配,努力让疫苗成为各国人民用得上、用得起的公共产品。”申博表示。
宇学峰对澎湃新闻(www.thepaper.cm)记者表示,“疫苗是一个全球的公共卫生产品,我们要考虑怎样能够尽量地生产出更多的产品,这确实是摆在所有生产企业面前的一个挑战,所以大家要共同去应对,包括生产方、监管方、储运方、使用方等,这个是一个很大的问题,需要大家一块去共同努力。”
在宇学峰看来,在某种程度上,新冠疫苗对中国的疫苗产业而言也是一次促进机会。在中国新冠患者几乎没有的情况下,中国团队需要采取国际多中心临床试验完成疫苗的后期试验,“不要说疫苗企业,包括其他中国药厂,在国际上做这种多中心临床,从资源、经验、布局都没有做过。尤其现在这种大流行的环境下,你要把所有的这些资源调动起来,它不是那么简单的事情。”
宇学峰同时表示,“即使不简单我们也要做,这也是我们学习的过程,是一个发展的过程。我相信这一次做完了,确实会对我们国内的疫苗产业是一个促进,是一个发展,这也是我们一直希望做到的。”而全球化的疫苗大国则不是一个产品两个产品能决定的,也不是一天两天能决定的。
(本文来自澎湃新闻,更多原创资讯请下载“澎湃新闻”APP)
 正在阅读:疫苗获批,中国全民免费接种:大流行终结开始?
正在阅读:疫苗获批,中国全民免费接种:大流行终结开始?